Острое влияние курения марихуаны и пероральное употребление дельта-9-тетрагидроканнабинола на специфическую проводимость дыхательных путей у пациентов с астмой.
РЕЗЮМИРУЯ:
Острые эффекты 2-процентной натуральной марихуаны (7 мг на кг) и 15 мг перорального дельта-9-тетрагидроканнабинола (ТГК) на плетизмографически определенную резистентность верхних дыхательных путей (RAw) и удельную проводимость дыхательных путей (SGaw) сравнивались с плацебо у 10 пациентов со стабильной бронхиальной астмой при использовании метода двойного слепого перекрёстного лечения. После выкуривания марихуаны SGaw сразу увеличивался и оставался значительно повышенным (на 33–48 процентов выше начальных контрольных значений) в течение как минимум 2 часов, тогда как SGaw не изменялся после плацебо. Пиковый бронхолитический эффект из 1250 мкг изопротеренола был более выраженным, чем у марихуаны, но эффект марихуаны длился дольше.
После приема 15 мг ТГК уровень SGaw значительно повышался через 1 и 2 часа, а уровень RAw значительно снижался через 1–4 часа, тогда как после приема плацебо никаких изменений не наблюдалось. Эти данные указывают на то, что у субъектов, страдающих астмой, при курении марихуаны, так и при пероральном приёме ТГК вызывали значительную бронхолитический эффект продолжительностью не менее 2 часов.
Вступление
В девятнадцатом веке одно из медицинских применений марихуаны было в терапии бронхиальной астмы; тем не менее, не было получено определенных доказательств её эффективности в качестве бронходилататора, пока недавние исследования не продемонстрировали значительную дилатацию дыхательных путей у здоровых молодых мужчин после курения марихуаны и приема его основного психоактивного ингредиента дельта-9-тетрагидроканнабинола (ТГК).
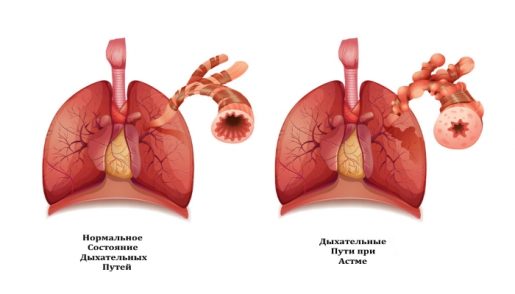 Вопрос о том, могут ли подобные эффекты быть вызваны у пациентов с бронхоспастическим заболеванием, представляет интерес, поскольку раздражающее действие дыма марихуаны, который, вероятно, является причиной симптомов бронхита, вызванных продолжительным или хроническим курением марихуаны, может перевесить бронхолитические свойства дельта-9-ТГК, что приводит к бронхоспазму у пациентов с гиперреактивными дыхательными путями. Следовательно, острый эффект от вдыхаемого дыма марихуаны и перорального введения дельта-9-ТГК на удельную проводимость дыхательных путей (SGaw) были исследованы в группе пациентов с клинически стабильной бронхиальной астмой.
Вопрос о том, могут ли подобные эффекты быть вызваны у пациентов с бронхоспастическим заболеванием, представляет интерес, поскольку раздражающее действие дыма марихуаны, который, вероятно, является причиной симптомов бронхита, вызванных продолжительным или хроническим курением марихуаны, может перевесить бронхолитические свойства дельта-9-ТГК, что приводит к бронхоспазму у пациентов с гиперреактивными дыхательными путями. Следовательно, острый эффект от вдыхаемого дыма марихуаны и перорального введения дельта-9-ТГК на удельную проводимость дыхательных путей (SGaw) были исследованы в группе пациентов с клинически стабильной бронхиальной астмой.
Материалы и методы
Испытуемые: Пять мужчин и 5 женщин (возрастом от 22 до 74 лет) с диагнозом бронхиальной астмы в соответствии с критериями, установленными Американским торакальным обществом. У каждого субъекта была клиническая особенность, которая характеризовалась типичными эпизодами хрипов, кашля и одышки, возникающими либо самопроизвольно, либо в ответ на воздействие вдыхаемых аллергенов или неспецифических раздражителей, эмоциональных аспектов, инфекций дыхательных путей или физических нагрузок, которые облегчались бронхолитическим средством.
На момент исследования все субъекты были клинически стабильны; астматические симптомы отсутствовали у 4 субъектов, хронические в легкой или средней степени тяжести у остальных. За исключением двух субъектов (PF и JBon), у которых, вероятно, кроме бронхоспастической болезни, была эмфизема легких, не было никаких признаков других значительных медицинских заболеваний по данным анамнеза, физикального обследования, общего анализа крови, химического анализа крови (SMA-12), клинического анализа мочи, электрокардиограмма и рентгенография грудной клетки. Значительное психическое заболевание было исключено на основании интервью с одним из исследователей и оценки результатов в многофазной инвентаризации личности в Миннесоте.
Все субъекты прошли обследования функции легких, включая спирометрию с использованием 13,5-литрового водного спирометра (Warren E. Collins, Inc.), способность к однократному дыханию для моноксида углерода (DLCO), сопротивление дыхательных путей (RAw) и объём лёгких (Vtg) с использованием 900-литрового плетизмографа для тела с переменным давлением. Чтобы оценить степень обратимой обструкции дыхательных путей, спирометрию выполняли как до, так и через 10 минут после вдыхания 0,25 мл изопротеренола HCL (1: 200) через небулайзер DeVilbiss, подключенный к дыхательному устройству с положительным давлением, работающим на сжатом воздухе.
Следующая методика была использована для введения изопротеренола аэрозоля. Пациентам было предложено сначала выдохнуть до остаточного объема, затем медленно вдохнуть из небулайзера до полной вместимости легких в течении приблизительно 10 секунд, а затем возобновить нормальное дыхание в течение нескольких секунд.
Эти маневры повторялись до тех пор, пока раствор бронхолитического средства в распылителе не был израсходован (обычно после 4-5 глубоких вдохов). Кроме того, RAw и Vtg измеряли как за 15 минут до и непосредственно перед ингаляцией изопротеренола, так и через 5, 15, 30 и 60 минут после бронходилататора. У всех субъектов потоки и SGaw (отношение обратной величины RAw к одновременно измеренному Vtg) увеличивались более чем на 25% после вдыхания изопротеренола, что указывает на чувствительность дыхательных путей к бронхолитическому лечению.
Семь из 10 субъектов ранее курили марихуану, но только время от времени (менее 1 косяка в месяц). Никто не признавался в употреблении наркотиков, отличных от тех, которые прописаны при бронхиальной астме, и никто не курил табак. Ни один субъект не использовал марихуану в течение 7 дней до настоящего исследования. Кроме того, бронхолитическое лечение было отменено по крайней мере за 8 часов до исследования.

Эксперименты проводились с каждым субъектом в 4 отдельных дня, начиная с 10 часов утра, с интервалом не менее 48 часов между каждой учебной сессией. Испытуемым сообщили, что они будут случайным образом получать марихуану или плацебо.
Курительная марихуана: в течение 2 из 4 экспериментальных сессий субъекты выкуривали 7 мг на кг массы тела натурального препарата марихуаны, содержащего либо 0,0% дельта-9-ТГК, служащего в качестве плацебо-контроля, либо 2 % дельта-9-ТГК в соответствии с случайный, двойным слепым перекрёстным исследованием; однако из-за сильных психотропных эффектов марихуаны было признано, что субъекты, вероятно, испытывали небольшие трудности в идентификации марихуаны.
Содержание ТГК в экспериментальном препарате ранее анализировали методом газожидкостной хроматографии (изучения физико-химических свойств). Препарат с 0% получали экстракцией активных каннабиноидов из природного материала до тех пор, пока все анализы на каннабинол, каннабидиол, дельта-8-ТГК и дельта-9-ТГК не составляли 0,0%.
В целях стандартизации количества летучего дельта-9-ТГК, поставляемого во вдыхаемом материале, использовалась методика равномерного курения. Субъекты глубоко вдыхали сигарету в течение 2-4 секунд, задерживали дыхание на 15 секунд, возобновляли нормальное дыхание в течение приблизительно 5 секунд, а затем повторяли эти маневры до тех пор, пока джоинт не догорал, в течение приблизительно 10 минут. Почти окурок держали щипцами, чтобы позволить почти полное употребление назначенного количества марихуаны, где сконцентрированы летучие каннабиноиды.
Следующие характеристики были измерены за 15 минут до и непосредственно перед курением марихуаны или плацебо (начальный контрольный период) и сразу же, через 5, 10, 15, 30, 60, 90, 120 и 180 минут после завершения курения: RAw, Vtg, частота дыхания, частота сердечных сокращений (определяется по электрокардиограмме), а также систолическое и диастолическое артериальное давление.
Кроме того, предоставить приблизительную оценку степени опьянения; в каждом интервале после курения марихуаны и плацебо 7 испытуемых, которые ранее имели опыт употребления каннабиса, просили оценить, насколько «кайфовали» они были по шкале от 0 до 7, где 7 представляли «самый мощный кайф», который они когда-либо чувствовали после курения марихуаны.
Продолжение исследования в следующей статье.